Ruolo di un nuovo acido
ialuronico 16mg/2ml
nel trattamento dell’osteoartrosi
Review della letteratura
a cura di Umberto Zoppi
Divisione di Ortopedia e Traumatologia, Ospedale Civile
di Teramo.
Introduzione
L’osteoartrosi è una delle patologie reumatiche
più comuni e diffuse nella popolazione ed è
una patologia cronica caratterizzata da una lenta e progressiva
degradazione della cartilagine articolare che provoca dolore
e aumento della disabilità motoria. Questa affezione
articolare può avere, soprattutto nei casi più
gravi, un pesante impatto sulla qualità di vita del
paziente comportando una limitazione funzionale e sociale.
Attualmente le opzioni terapeutiche utilizzate sono rappresentate
in prima istanza da farmaci antinfiammatori e analgesici
sistemici e topici e da infiltrazioni intraarticolari di
corticosteroidi e acido ialuronico.
Ruolo dell’acido ialuronico nell’articolazione
osteoartrosica
Il trattamento intraarticolare con acido ialuronico è
entrato solo di recente a pieno diritto nell’armamentario
terapeutico per il trattamento dell’osteoartrosi,
in quanto numerosi studi ne hanno dimostrato l’efficacia
viscoelastica, lubrificante e antiinfiammatoria svolta nell’articolazione
osteoartrosica.
Infatti, se si considera che l’acido ialuronico rappresenta
uno dei più importanti componenti del corpo umano
trovandosi, praticamente, in tutti i tessuti, ben si può
comprendere l’importanza che assume all’interno
della cartilagine e, in dettaglio, nel liquido sinoviale,
il quale deve le sue caratteristiche ammortizzanti, lubrificanti
e antinfiammatorie proprio all’acido ialuronico endogeno.
Tuttavia, in corso di patologia artrosica il liquido sinoviale
si altera e di conseguenza si riduce la concentrazione e
la qualità dell’acido ialuronico nell’articolazione;
inoltre, la membrana sinoviale diventa più permeabile
favorendo il passaggio di sostanze pro-infiammatorie.
In sintesi, in una cartilagine osteoartrosica avviene uno
sbilanciamento del delicato equilibrio esistente tra sintesi
e degradazione della matrice cartilaginea. In corso di osteoartrosi,
l’equilibrio tra sintesi e degradazione si sposta
verso quest’ultima, come illustrato in figura 1.
Figura 1. Alterazione
dell’equilibrio tra degradazione e sintesi di matrice
cartilaginea in corso di OA
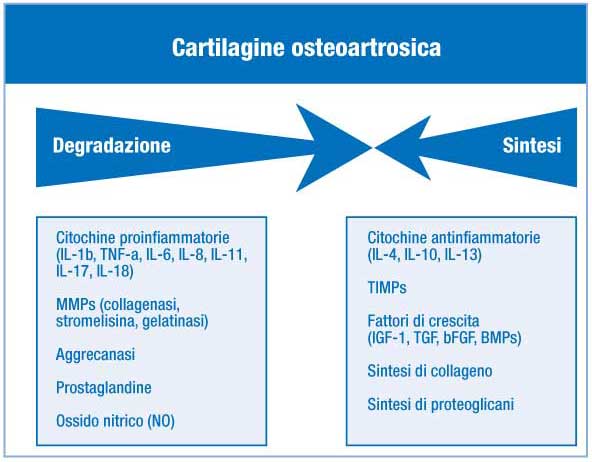
Figura 2. Stimolazione
percentuale della sintesi di acido ialuronico endogeno
in cellule cartilaginee osteoartrosiche.
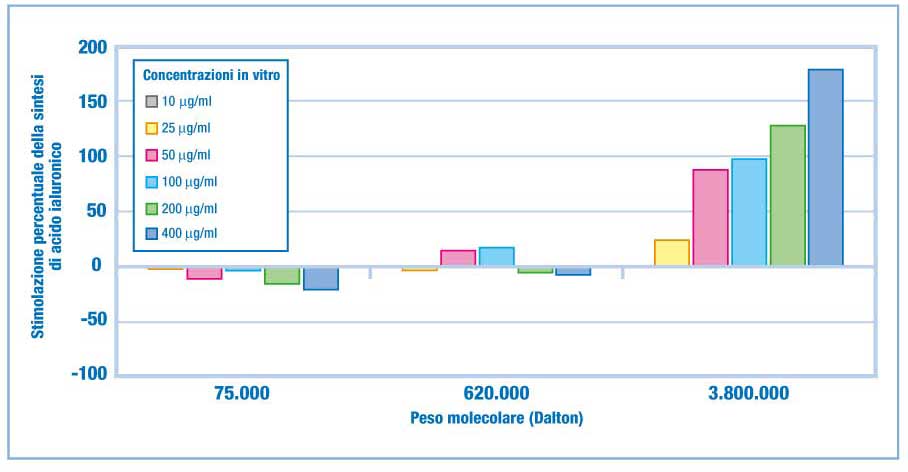
Figura 3. Affinità
recettoriale e stimolazione endogena di acido ialuronico
con peso molecolare differente.

Figura 4. Cellula sinoviale
in coltura circondata da acido ialuronico
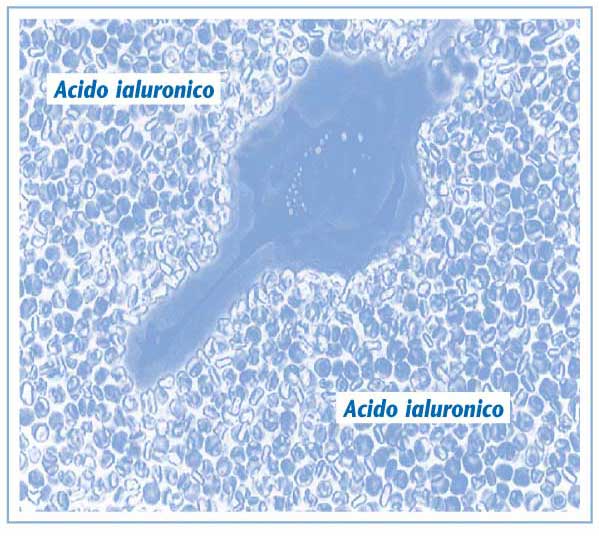
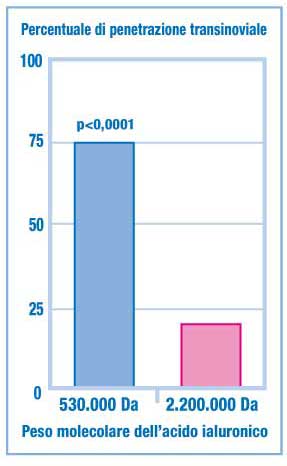
Figura 5. Percentuale
di penetrazione transinoviale di acido ialuronico
top
L’acido ialuronico endogeno è responsabile
delle proprietà viscoelastiche del liquido sinoviale
e agisce sia come lubrificante che come ammortizzatore degli
urti; riveste tutta la superficie della cartilagine articolare
e blocca la migrazione di proteoglicani dalla matrice cartilaginea
all’interno dello spazio sinoviale mantenendo normale
la matrice stessa. Allo stesso modo l’acido ialuronico
sembra impedisca l’invasione di cellule proinfiammatorie
all’interno dello spazio e del liquido articolare.
Tuttavia, in corso di processi infiammatori acuti e cronici
dell’articolazione, la dimensione delle molecole di
acido ialuronico si riduce, favorendo il passaggio di sostanze
proinfiammatorie e degradative della cartilagine.
Da queste considerazioni deriva l’obiettivo di ristabilire
il volume del liquido sinoviale rispettando e reintegrando
le sue proprietà viscoelastiche e lubrificanti, stimolando
la produzione di nuovo acido ialuronico endogeno ad azione
antiinfiammatoria e analgesica, attraverso le infiltrazioni
intraarticolari.
Le numerose evidenze scientifiche sull’importanza
dell’acido ialuronico nella terapia dell’osteoartrosi
hanno portato alla ricerca di nuove molecole caratterizzate
da un peso molecolare ideale, tale cioè da consentire
all’acido ialuronico di svolgere funzioni viscoelastiche,
lubrificanti e antinfiammatorie.
Tuttavia non tutti gli acidi ialuronici sono uguali e si
differenziano principalmente per due aspetti: la biotecnologia
alla base della loro sintesi e/o estrazione e il peso molecolare.
L’acido ialuronico può essere prodotto attraverso
l’estrazione da creste di gallo o per fermentazione
batterica, una biotecnologia di recente sviluppo.
Tabella 1. Effetto dell’acido
ialuronico sui principali mediatori dell’infiammazione
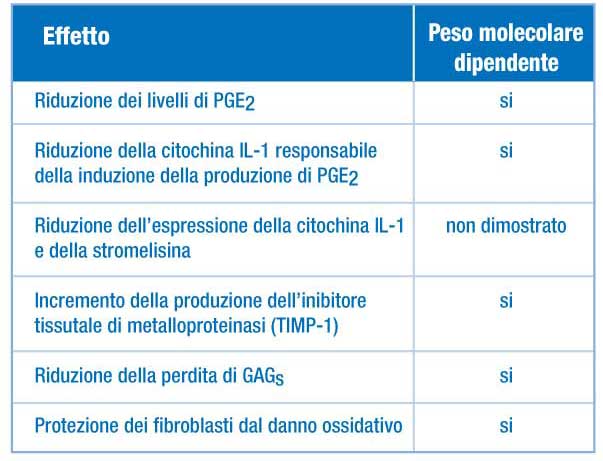
Tabella 2. Attività
di un nuovo acido ialuronico 16mg/2ml

I recenti avvenimenti in merito alla diffusione di malattie
animali nell’uomo, come l’attuale virus della
influenza aviaria, hanno portato la ricerca scientifica
a concentrarsi su biotecnologie atte a ottenere l’acido
ialuronico per fermentazione batterica, una tecnica, appunto,
che assicura la totale purezza della sostanza senza alcun
rischio di contaminazione da molecole o virus di provenienza
animale evitando l’insorgenza di allergie nei pazienti.
Recentemente è stato introdotto in commercio un acido
ialuronico ottenuto per fermentazione batterica e non estratto
da creste di gallo.
Se le metodiche di produzione sono ormai consolidate, occorre
invece fare una maggiore chiarezza relativamente al peso
molecolare dell’acido ialuronico e all’importanza
che esso ha nel garantire l’efficacia nel tempo delle
infiltrazioni intraarticolari.
Infatti, è stato accertato, attraverso numerosi studi,
che la sintesi di nuovo acido ialuronico endogeno è
influenzata dalla concentrazione e dal peso molecolare dell’acido
ialuronico introdotto con metodica infiltrativa intraarticolare.
È ormai dimostrato che l’acido ialuronico,
per poter esplicare le sue attività intrinseche nella
cartilagine artrosica, deve necessariamente legarsi in maniera
forte e ottimale con i recettori specifici (CD44) situati
sulla superficie della membrana sinoviale, in maniera tale
da stimolare la cellula a trasmettere tutti quei segnali
biochimici necessari alla stimolazione endogena. Inoltre,
è stato osservato che più il legame recettoriale
con l’acido ialuronico endogeno è forte, maggiore
sarà la permanenza dello stesso nel liquido sinoviale
e più duraturo sarà l’effetto di stimolazione.
Studi in vitro hanno dimostrato che un acido ialuronico
con basso peso molecolare (<0,5x106 Dalton) presenta
una bassa affinità con i recettori cellulari per
l’acido ialuronico con la conseguenza di non stimolare
o stimolare solo parzialmente la biosintesi di acido ialuronico
endogeno. Allo stesso modo, un acido ialuronico ad elevato
peso molecolare (>4,0x106 Dalton) presenta un ingombro
sterico tale da non consentire o consentire solo in parte
il legame recettoriale e, anche in questo caso, la conseguenza
è rappresentata dalla scarsa stimolazione della sintesi
da parte dei fibroblasti.
Allo scopo di approfondire queste osservazioni, alcuni ricercatori
hanno realizzato uno studio in vitro su cellule cartilaginee
osteoartrosiche, reumatoidi e normali per verificare quale
peso molecolare sia più in grado di stimolare la
sintesi di acido ialuronico endogeno.
Utilizzando varie preparazioni di acido ialuronico con differente
peso molecolare (da un minimo di 0,075x106 Dalton ad un
massimo di 3,8x106 Dalton) e con differenti concentrazioni
(10µg/ml, 25µg/ml, 50µg/ml, 100µg/ml,
200µg/ml e 400µg/ml) hanno valutato la capacità
del preparato di indurre la stimolazione endogena.
Dall’analisi dei dati è emerso che una concentrazione
in vitro di circa 200µg/ml è quella più
simile a quella che si otterrebbe con una infiltrazione
intrarticolare in vivo.
Dal punto di vista della pratica clinica tale dato (riportato
in figura 2) può essere importante in quanto influisce
sulla scelta dell’acido ialuronico da utilizzare per
l’infiltrazione intraarticolare: infatti, uno dei
primi prodotti a base di acido ialuronico più diffuso
in Italia ha un peso molecolare di circa 0,62x106 Dalton,
non in grado, quindi, di stimolare la sintesi endogena,
come del resto è chiaramente evidenziato in figura
2.
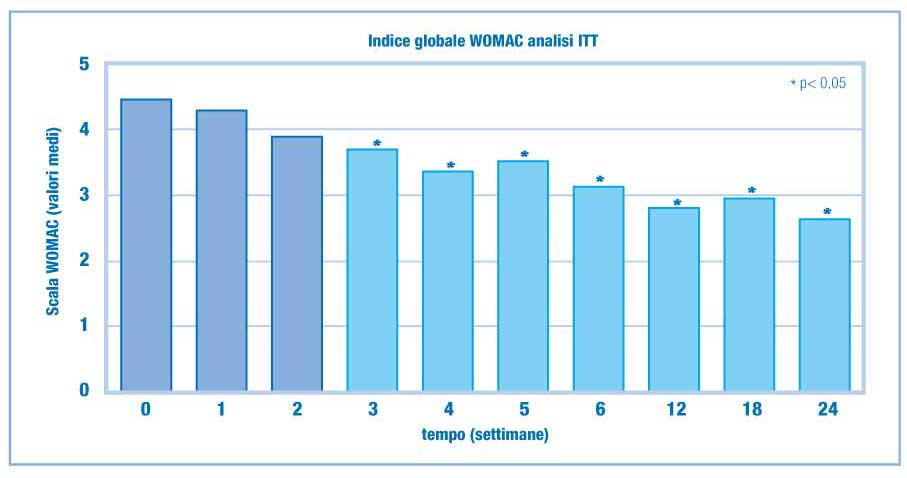
Figura 6. Miglioramento
della mobilità articolare e della sintomatologia
dolorosa valutate tramite indice algo-funzionale WOMAC ottenuto
con un nuovo acido ialuronico 16mg/2ml.
top
La conclusione di tale studio indica che la sintesi endogena
viene stimolata a partire da un peso molecolare di 0,88x106
Dalton, mentre gli altri acidi ialuronici presi in esame
e con peso molecolare inferiore, non stimolano la sintesi
endogena in nessuna delle tre linee cellulari studiate (osteoartrosica,
reumatoide e normale).
Analisi effettuate su colture di cellule estratte da cartilagini
articolari osteoartrosiche, hanno, infine, identificato
che il peso molecolare ideale per un acido ialuronico è
rappresentato da un peso compreso tra 0,5x106 e 4,0 x106
Dalton; tale peso sembra essere, infatti, quello caratterizzato
da una forte affinità recettoriale e, quindi, da
una maggiore e ottimale stimolazione di acido ialuronico
endogeno. (Figura 3)
Tuttavia, l’attività dell’acido ialuronico
non può essere confinata alla sola stimolazione endogena;
infatti, è stato dimostrato che l’acido ialuronico
possiede un effetto antiinfiammatorio: ancorandosi ai recettori
cellulari, circonda la cellula sinoviale creando una sorta
di barriera che riduce le interazioni tra le sostanze proinfiammatorie
penetrate nel liquido sinoviale e la cellula stessa, riducendo
lo stato infiammatorio articolare. (Figura 4)
Figura 7. Valutazione
dello sperimentatore sulla tollerabilità e sicurezza
di un nuovo ac. ialuronico 16mg/2ml al termine dello studio.
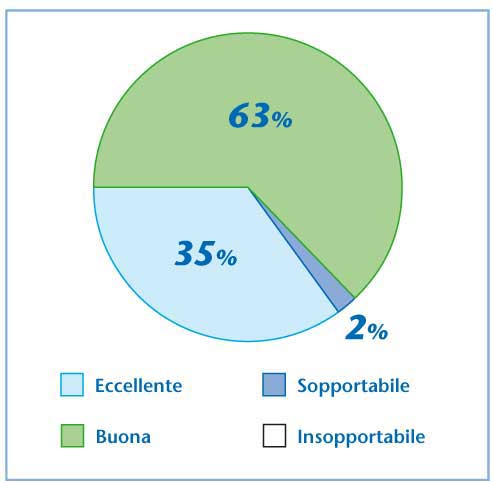
Figura 8. Miglioramento
della funzionalità articolare ottenuto con un nuovo
ac. ialuronico 16mg/2ml valutata tramite indice di Lequesne.
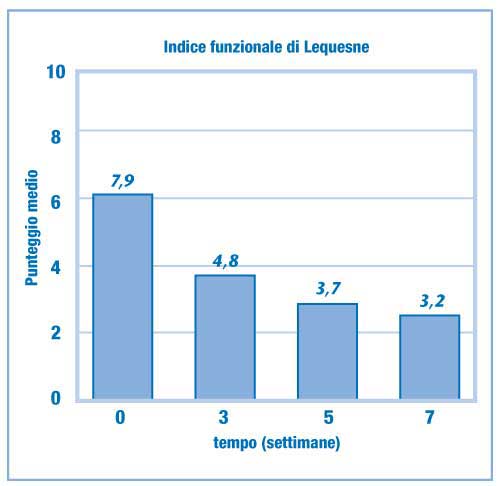
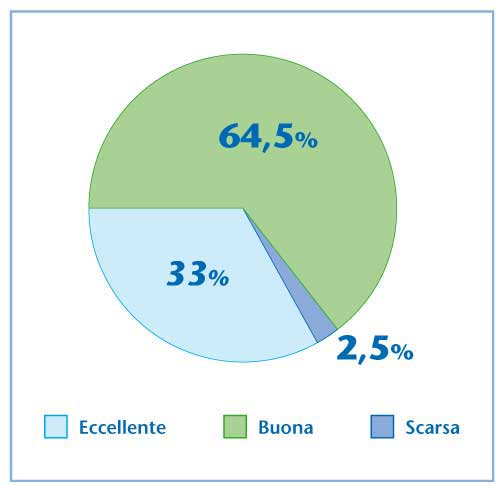
Figura 9. Valutazione
dello sperimentatore e del paziente sulla tollerabilità
di un nuovo ac. ialuronico 16mg/2ml al termine dello studio.
Tale affermazione trova riscontro in numerosi studi in vivo
dove è stata osservata una attività antiinfiammatoria
dipendente dal peso molecolare. In particolare è
stato visto un effetto inibitorio sui neutrofili attivati
responsabili della degradazione della cartilagine, espresso
come riduzione della perdita di glicosaminoglicani, risultato
peso molecolare dipendente. Rispetto ad un acido ialuronico
di basso peso molecolare, i dati illustrano come la riduzione
della perdita di glicosaminoglicani sia maggiore con acido
ialuronico di peso molecolare di 0,95x106 Da.
Inoltre, è stato visto che l’acido ialuronico
presenta un’attività peso molecolare dipendente
nei confronti delle reazioni indotte da radicali liberi
e altri mediatori della flogosi, proteggendo, pertanto,
i tessuti cartilaginei dal danno ossidativo.
A tale riguardo i dati permettono di affermare che una preparazione
di acido ialuronico con peso molecolare di 1,2x106 Da è
più efficace nel proteggere i fibroblasti dal danno
ossidativo rispetto a un acido ialuronico di peso molecolare
di 0,176x106Da o di 0,668x106 Da.
Gli ulteriori effetti antinfiammatori dell’acido ialuronico,
somministrato per via intraarticolare, rappresentati in
tabella 1, sono essenzialmente dovuti all’attività
sui principali mediatori della flogosi, che, in caso di
articolazione osteoartrosica, penetrano all’interno
della stessa aumentando il danno, l’infiammazione
e la degradazione della cartilagine. (Tabella 1)
Tutte queste evidenze sull’attività dell’acido
ialuronico sono strettamente dipendenti dalla capacità
dello stesso di penetrare all’interno del liquido
transinoviale.
Infatti, le concentrazioni transinoviali indicano la capacità
di penetrare la matrice extracellulare e, di conseguenza,
la percentuale di sostanza in grado di raggiungere i recettori
cellulari per l’acido ialuronico.
In uno studio sperimentale effettuato in vivo, è
stato appurato che esiste una stretta relazione tra il peso
molecolare dell’acido ialuronico e la sua capacità
di penetrare il fluido transinoviale; i dati raccolti hanno
permesso di evidenziare come un acido ialuronico di peso
molecolare superiore o uguale a 2,2x106 Da non sia in grado
di garantire concentrazioni transinoviali significative.
(Figura 5)
Anche questo dato presenta un aspetto pratico, in quanto,
evidenzia come un acido ialuronico ad elevato peso molecolare
presenti una scarsa penetrazione transinoviale, comportando
quindi una minore stimolazione endogena e una ridotta capacità
di intervenire sui processi infiammatori provocati dai modulatori
della flogosi, mentre un acido ialuronico di basso peso
molecolare (0.5x106 Da) presenti una elevata penetrazione
transinoviale ma anche uno scarso legame con i recettori
e, di conseguenza, non sia in grado di stimolare alcuna
biosintesi endogena.
top
Risvolti clinici
Curiosamente, per riscontrare le prime evidenze cliniche
sull’utilizzo dell’acido ialuronico occorre
risalire a studi sugli animali: infatti, proprio per le
attività descritte precedentemente, i primi impieghi
dell’acido ialuronico sono stati effettuati sui cavalli
da corsa, dove la necessità di mantenere efficienti
le articolazioni rappresentava più un obiettivo economico
(le corse dei cavalli hanno un giro d’affari estremamente
importante) che non legato al bisogno di sperimentazioni
vere e proprie sull’animale.
È proprio dai successi terapeutici ottenuti nei cavalli
da corsa che la medicina e la ricerca scientifica medica
hanno iniziato a studiare gli effetti dell’acido ialuronico
nelle articolazioni dell’uomo, approfondendo nel tempo
tutti i suoi possibili effetti ed attività nella
cartilagine articolare.
A seguito di numerosi studi clinici effettuati nell’uomo,
la terapia infiltrativa intraarticolare di acido ialuronico
è oggi entrata a far parte del bagaglio terapeutico
del medico; in particolare, i successi ottenuti nel trattamento
dell’osteoartrosi del ginocchio hanno contribuito
alla diffusione dell’utilizzo clinico dell’acido
ialuronico.
I successi clinici riscontrati nelle articolazioni osteoartrosiche,
hanno stimolato la ricerca e la commercializzazione di nuovi
prodotti biotecnologicamente più avanzati. È
di recente immissione in commercio una nuova soluzione di
acido ialuronico fisiologico tamponato a base di ialuronato
di sodio (sale sodico dell’acido ialuronico) altamente
purificato allo 0,8%, ottenuto per fermentazione batterica
e caratterizzato da un peso molecolare che, alla luce delle
evidenze sperimentali in vitro e in vivo precedentemente
trattate, si presenta come ideale.
Il peso molecolare di questo nuovo acido ialuronico è,
infatti, compreso tra 0,8x106 Da e 1,2x106 Da, il che lo
colloca esattamente all’interno del range definito
ideale dalla letteratura internazionale di 0,5x106 Da-4,0x106
Da.
Di conseguenza presenta una serie di attività che
lo rendono ideale nel trattamento dell’osteoartrosi
ripristinando l’equilibrio tra sintesi e degradazione
della matrice cartilaginea e riducendo il catabolismo della
cartilagine stessa. (Tabella 2)
Dal punto di vista dell’efficacia terapeutica, questa
nuova soluzione di acido ialuronico è stata oggetto
di un’attenta valutazione clinica della quale vengono
qui citati due studi effettuati su pazienti affetti da osteoartrosi
al ginocchio, l’articolazione più diffusamente
colpita da questa patologia.
top
Il primo studio clinico aveva l’obiettivo di valutare
l’efficacia e la tollerabilità di questa nuova
soluzione su 63 pazienti di età compresa tra i 18
e 85 anni, trattati ambulatorialmente per gonartrosi cronica;
all’arruolamento i pazienti manifestavano una sintomatologia
dolorosa di almeno 30 mm su Scala Analogico Visiva (VAS)
di 100 mm. I risultati dello studio hanno dimostrato come
i punteggi dell’indice algo-funzionale WOMAC (Western
Ontario and McMaster University Osteoarthritis) relativi
a dolore, rigidità e mobilità articolare,
si siano ridotti in maniera statisticamente significativa
a partire dalla 3° settimana di trattamento (Figura
6) .
La tollerabilità e la sicurezza di questo nuovo acido
ialuronico sono state valutate sulla base dei sintomi osservati
e riguardanti dolore nel sito di iniezione ed eventi avversi
dopo il trattamento, che, secondo il giudizio dello sperimentatore,
sono risultate eccellenti nella maggioranza dei pazienti
(Figura 7).
Il secondo studio è stato condotto per verificare
l’effetto del trattamento con questa nuova soluzione
di acido ialuronico in 40 pazienti ambulatoriali di età
compresa tra 18 e 82 anni con compromissione articolare
del ginocchio; dai risultati ottenuti è stata osservata
una progressiva riduzione del punteggio dell’indice
di Lequesne confermando, di conseguenza, l’efficacia
del trattamento. Il punteggio dell’indice di Lequesne
è stato così considerato: 8-10 artrosi grave;
5-7 artrosi moderata; 1-4 artrosi lieve. (Figura 8)
Come nel precedente studio, la tollerabilità locale
e sistemica secondo la valutazione dello sperimentatore
e del paziente è stata giudicata eccellente nella
maggior parte dei casi. (Figura 9)
Conclusioni
A conclusione di questa revisione della letteratura si può
affermare che, grazie ai numerosi studi che approfondiscono
i meccanismi biologici e biochimici che sono alla base della
efficacia terapeutica nell’osteoartrosi, i preparati
a base di acido ialuronico possono rientrare nelle opportunità
terapeutiche a disposizione del medico curante.
Tuttavia, poiché come si è visto, non tutti
i preparati disponibili sono uguali, è necessario
che il medico ponga una certa attenzione nella scelta del
prodotto da infiltrare, tenendo presente che le differenze
che li contraddistinguono, possono dare risultati terapeutici
differenti e in alcuni casi possono disattendere le aspettative.
Pertanto, in tutti i pazienti con danno articolare avanzato,
in fase di recupero funzionale, affetti da osteoartrosi
o che hanno subito traumi articolari, la scelta dovrebbe
indirizzarsi verso una preparazione di acido ialuronico
che abbia un peso molecolare ideale (0,8x106 Da - 1,2x106
Da), ottenuto per fermentazione batterica e non per estrazione
da creste di gallo e abbia dimostrato di assicurare il ripristino
sia delle proprietà reologiche del liquido sinoviale
sia dell’equilibrio endogeno tra sintesi e degradazione
della matrice cartilaginea.
top
Bibliografia essenziale
• Altman RD. Status of hyaluronan supplementation
therapy in osteoarthritis. Curr Rheumatol Rep. 2003 Feb;5(1):7-14.
• Castellacci E, et al. Antalgic effect and clinical
tolerability of hyaluronic acid in patients with degenerative
diseases of knee cartilage: an outpatient treatment survey.
Drugs Exp Clin Res. 2004;30(2):67-73
• Coleman PJ, et al. Role of hyaluronan chain length
in buffering interstitial flow across synovium in rabbits.
J Physiol. 2000 Jul 15;526 Pt 2:425-34
• Ghosh P, et al. Potential mechanism of action of
intra-articular hyaluronan therapy in osteoarthritis: are
the effects molecular weight dependent? Semin Arthritis
Rheum. 2002 Aug;32(1):10-37.
• Kelly MA, et al. Intra-articular hyaluronans in
knee osteoarthritis: rationale and practical considerations.
Am J Orthop. 2004 Feb;33(2 Suppl):15-22.
• Kuiper-Geertsma DG, et al. Intra-articular injection
of hyaluronic acid as an alternative option to corticosteroid
injections for arthrosis. Ned Tijdschr Geneeskd. 2000 Nov
11;144(46):2188-92.
• Laurent TC, et al. Hyaluronan. FASEB J. 1992 Apr;6(7):2397-404.
• Lequesne MG, et al. Indexes of severity for osteoarthritis
of the hip and knee.Validation-value in comparison with
other assessment tests. Scand J Rheumatol Suppl. 1987;65:85-9.
• Michel BA, et al. In press.
• Moreland LW. Intra-articular hyaluronan (hyaluronic
acid) and hylans for the treatment of osteoarthritis: mechanisms
of action. Arthritis Res Ther. 2003;5(2):54-67.
• Moskowitz RW, et al. Understanding osteoarthritis
of the knee-causes and effects. Am J - Orthop. 2004 Feb;33(2
Suppl):5-9
• Moskowitz RW. Hyaluronic acid supplementation. Curr
Rheumatol Rep. 2000 Dec;2(6):466-71.
• Pelletier JP, et al.The pathophysiology of osteoarthritis
and the implication of the use of hyaluronan and hylan as
therapeutic agents in viscosupplementation. J Rheumatol
Suppl. 1993 Aug;39:19-24.
• Pleimann JH, et al. Viscosupplementation for the
arthritic ankle. Foot Ankle Clin. 2002 Sep;7(3):489-94.
• Presti D, et al. Hyaluronan-mediated protective
effect against cell damage caused by enzymatically produced
hydroxyl (OH) radicals is dependent on hyaluronan molecular
mass. Cell Biochem Funct 1994;12:281-8.
• Smith MM, et al. The synthesis of hyaluronic acid
by human synovial fibroblasts is influenced by the nature
of the hyaluronate in the extracellular environment.Rheumatol
Int. 1987;7(3):113-22
top